近年來,寡核苷酸藥物作為一種新型治療手段發展迅速,在罕見病、心血管疾病、自身免疫性疾病及代謝性疾病領域展現出廣闊的治療前景。隨著研究的深入,監管機構已針對寡核苷酸藥物的非臨床安全性評價及臨床藥理研究發布了相關指導原則[1]-[2],但目前尚無專門針對其非臨床藥代動力學(DMPK)研究的相關指南。因此,如何設計并開展支持新藥申報(IND/NDA)的體外代謝研究,仍是研發人員關注的重點。
對于寡核苷酸藥物,其在體內循環系統及靶組織中的穩定性及暴露形式是影響其安全性和有效性的關鍵因素,需通過體內外代謝研究提供數據支持。本文針對寡核苷酸藥物的特性、作用機制及已上市產品的研究經驗,系統探討其體外代謝研究的策略和方法。
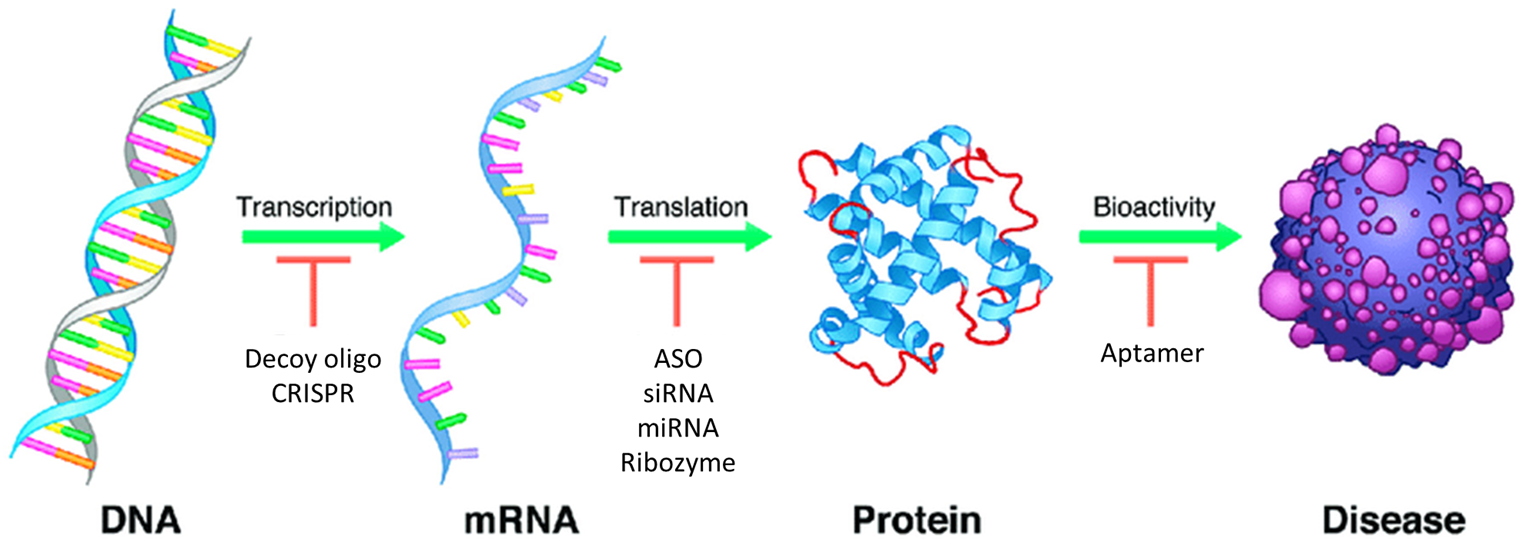
寡核苷酸藥物是由人工化學合成的12~30個核苷酸的單鏈或雙鏈分子。與傳統小分子和抗體藥物不同,其通過堿基互補配對原理,特異性結合內源性核酸序列,在mRNA水平上調控基因表達,從而實現疾病治療[3]。主要類型包括小干擾RNA(siRNA)、反義寡核苷酸(ASO)、微小RNA(miRNA)等。
此類藥物具有靶向特異性強、毒性較低、研發成功率較高等優勢,且可作用于傳統藥物難以靶向的治病基因。然而,其高極性、強負電荷及易被核酸酶降解等特性,顯著限制了成藥性。為此,通常需要采用化學修飾和遞送系統進行優化。
常見的化學修飾包括:骨架修飾(如硫代磷酸酯,PS);糖環修飾(如2’-O-甲基、2’-氟、鎖核酸LNA);堿基修飾;末端修飾。
遞送系統方面,肝靶向技術最為成熟,主要包括脂質納米顆粒(LNP)和N-乙酰半乳糖胺(GalNAc)偶聯技術。隨著遞送技術的研究深入,肝外靶向遞送技術成為熱點,策略包括:配體偶聯(如膽固醇、長鏈脂肪酸等);抗體、多肽偶聯;外泌體等新型載體。
寡核苷酸藥物主要經血漿和組織中廣泛存在的核酸內切酶和核酸外切酶代謝,而非依賴肝臟的Ⅰ相和Ⅱ相代謝酶[3]-[4]。若采用特殊遞送系統(如LNP、脂肪酸偶聯物),其載體部分可能經肝臟的Ⅰ相和Ⅱ相代謝酶代謝,需予以考慮。其中,核酸外切酶從鏈末端逐個切除核苷酸,而核酸內切酶在鏈內部切割,產生不同長度的片段。
體外代謝研究在寡核苷酸藥物開發中具有三大核心價值:
需注意,與化學小分子藥物不同,寡核苷酸藥物的代謝研究一般不用于種屬選擇,因其非臨床動物種屬主要依據靶序列同源性確定。
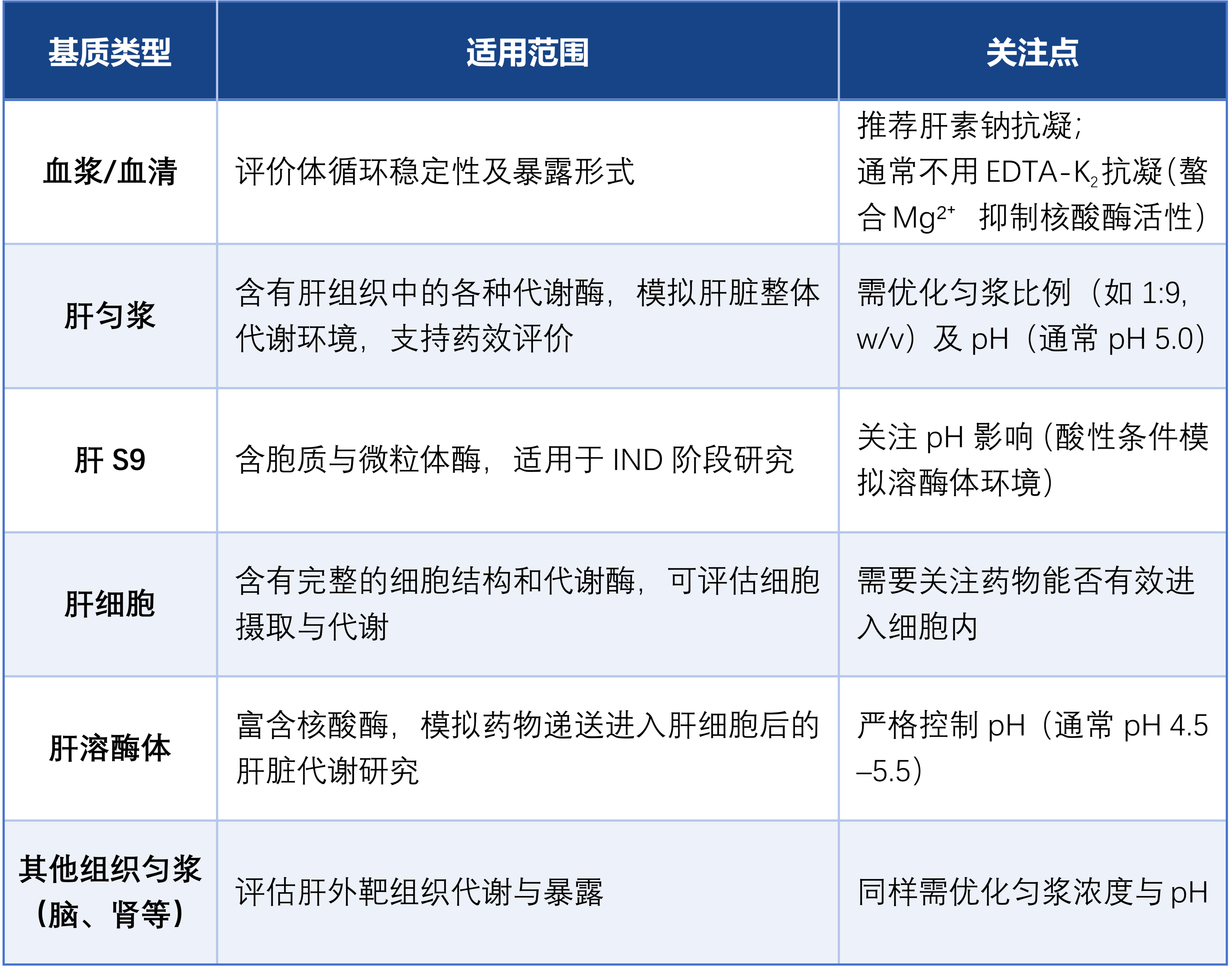
常用體外代謝體系如下表所示:
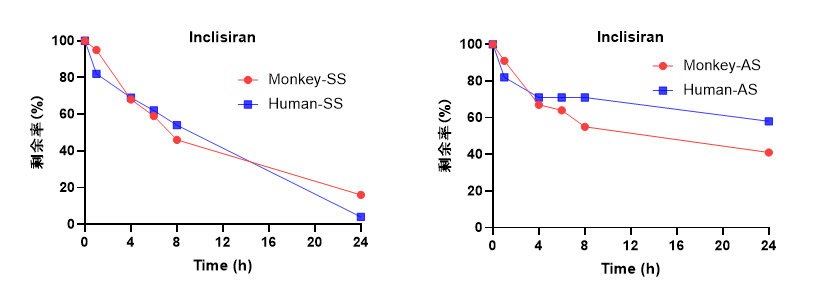
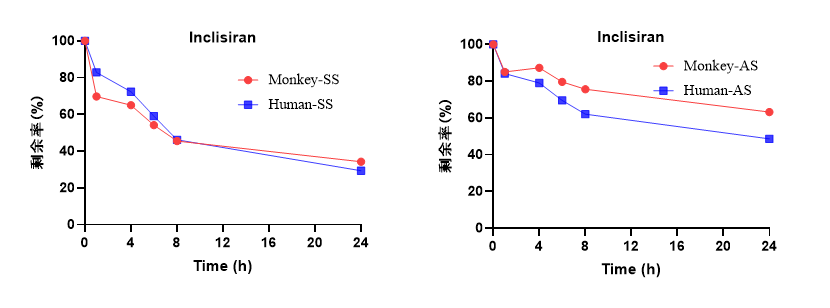
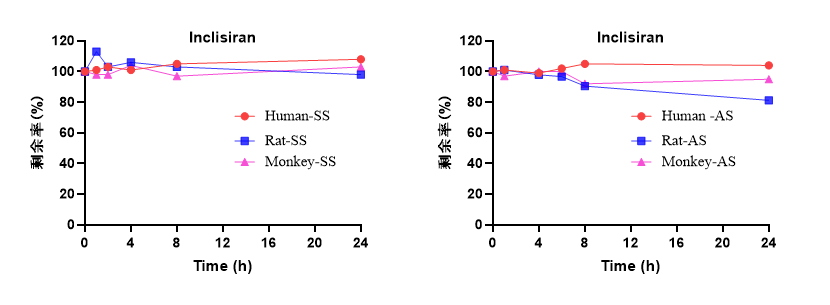
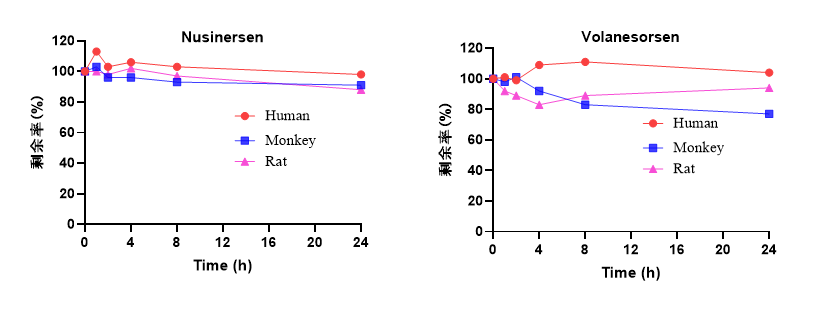
當前已上市的寡核苷酸藥物多以肝臟為靶點,且肝臟是最重要的代謝器官,故代謝研究常聚焦肝相關基質(肝勻漿、肝S9)及血漿。隨著肝外靶向藥物的發展,基于藥物的作用部位、給藥途徑等合理選擇代謝基質,如CNS藥物通常擴展至腦組織勻漿、腦脊液等基質。本文主要探討基于肝組織(肝勻漿、肝S9)及血漿的體外代謝研究策略。肝勻漿保留肝臟全部亞細胞結構及酶系,能最全面模擬肝內代謝環境,適用于早期候選物篩選。孵育液的pH、勻漿液濃度是重點考察條件。本研究優化孵育條件為pH5.0、1:9 (g: mL)勻漿比例,考察陽性藥Inclisiran在食蟹猴和人肝勻漿中的代謝。結果顯示,Inclisiran在肝勻漿體系37℃孵育24 h后,藥物發生明顯代謝消除,正義鏈(SS)的代謝速率高于反義鏈(AS),種屬間無顯著代謝差異(圖1)。圖1. Inclisiran在食蟹猴和人肝勻漿中的代謝穩定性肝S9包含胞質和微粒體組分,操作簡便,易于獲取,常用于IND申報階段。與肝勻漿體系的建立類似,由于寡核苷酸藥物本身的代謝特性與小分子不同,肝S9的濃度、孵育體系pH值通常對試驗結果產生影響。在pH5.0、2 mg/mL蛋白濃度下,37℃孵育24 h,陽性藥Inclisiran在食蟹猴和人肝S9中同樣呈現時間依賴性代謝消除,正義鏈(SS)的代謝速率高于反義鏈(AS)(圖2)。圖2. Inclisiran在食蟹猴和人肝S9中的代謝穩定性與寡核苷酸穩定性直接相關的核酸酶在血液中大量分布,血漿穩定性考察對早期候選物篩選研究至關重要。由于EDTA可抑制核酸酶的活性,通常選用肝素鈉抗凝的血漿考察寡核苷酸藥物的穩定性。對多種已上市的寡核苷酸藥物的測試表明,37℃孵育24 h后,其在人、猴、大鼠血漿中均保持較高穩定性,種屬差異較小(圖3)。圖3. 不同寡核苷酸藥物在SD大鼠、食蟹猴和人血漿中的代謝穩定性寡核苷酸藥物的天然結構易被生物體系中的核酸酶快速降解,是導致其體內半衰期短、生物利用度低的主要原因。因此,評估并優化其代謝穩定性是早期發現階段的核心任務。有濟醫藥已建立涵蓋血漿/血清、肝勻漿、肝S9、肝溶酶體、肝細胞、腎勻漿等多種體外研究模型,可為寡核苷酸候選化合物的篩選優化及臨床試驗設計提供全方位技術支持。
[1]FDA Guidance for Industry: Nonclinical Safety Assessment of Oligonucleotide-Based Therapeutics, November 2024.[2]FDA Guidance for Industry: Clinical Pharmacology Considerations for the Developments of Oligonucleotide Therapeutics, June 2024[3]Berman, C. L., Aldinger, M., Bauss. OSWG recommended approaches to the nonclinical pharmacokinetic (ADME) characterization of therapeutic oligonucleotides. Nucleic Acid Therapeutics. 2023, 33(5), 287–305.[4]Migliorati, J. M., Liu, S., Liu, A. Absorption, distribution, metabolism, and excretion of FDA-approved antisense oligonucleotide drugs. Drug Metabolism and Disposition, 2022, 50 (7), 888–897.