在臨床生物樣品分析領(lǐng)域,法規(guī)的遵循與技術(shù)的精準(zhǔn)度同等重要。每一次法規(guī)的更新,都是行業(yè)發(fā)展道路上的新標(biāo)識(shí)。
2025年全球生物分析法規(guī)持續(xù)變革,迎來(lái)了多個(gè)重要?jiǎng)討B(tài),這些動(dòng)態(tài)與現(xiàn)行的ICH M10落地緊密相關(guān)。以下將以ICH M10為對(duì)照,對(duì)全球生物分析法規(guī)進(jìn)行深入剖析。
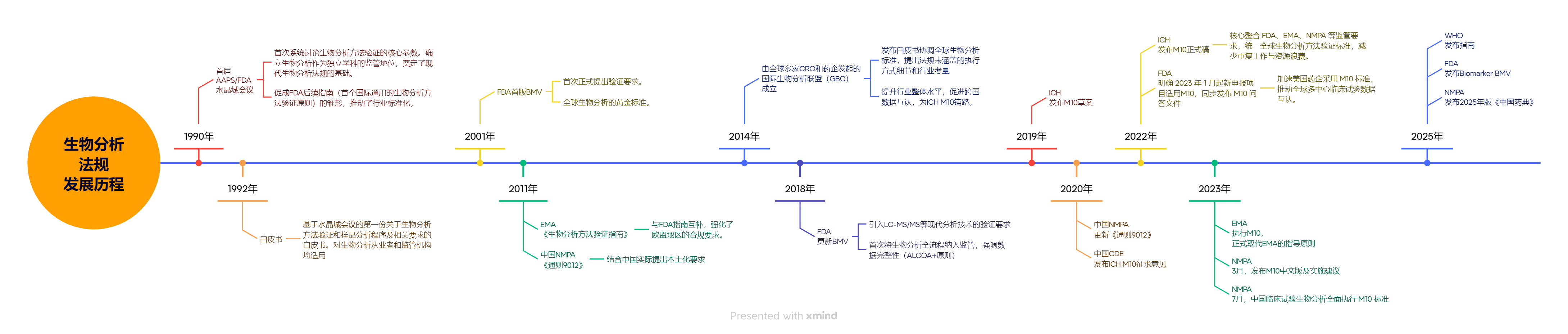
FDA新規(guī):BMV落幕,M10全面主導(dǎo)
中國(guó)藥典新動(dòng)向:9012退場(chǎng),接軌國(guó)際標(biāo)準(zhǔn)
在很長(zhǎng)一段時(shí)間里,9012從國(guó)內(nèi)藥品研發(fā)和檢測(cè)的實(shí)際情況出發(fā),對(duì)規(guī)范臨床生物樣品分析發(fā)揮了重要作用。不過(guò)9012和M10兩者確實(shí)存在很多差異,如今9012正式退場(chǎng),也促使了國(guó)內(nèi)臨床生物樣品檢測(cè)機(jī)構(gòu)全面對(duì)標(biāo)國(guó)際先進(jìn)標(biāo)準(zhǔn),審視現(xiàn)有檢測(cè)流程和質(zhì)量體系,進(jìn)一步提升自身在國(guó)際市場(chǎng)的競(jìng)爭(zhēng)力,更好地服務(wù)于全球藥品研發(fā)。
上述兩項(xiàng)內(nèi)容可視為2022年各主要藥監(jiān)機(jī)構(gòu)支持M10落地后,區(qū)域性法規(guī)隨之進(jìn)行適應(yīng)性調(diào)整所產(chǎn)生的后續(xù)影響。接下來(lái),世界衛(wèi)生組織(WHO)的文件則是在M10的基礎(chǔ)上,針對(duì)一些細(xì)節(jié)作出更為明確的規(guī)定。
WHO發(fā)布新指導(dǎo)原則:這些細(xì)節(jié)不容忽視
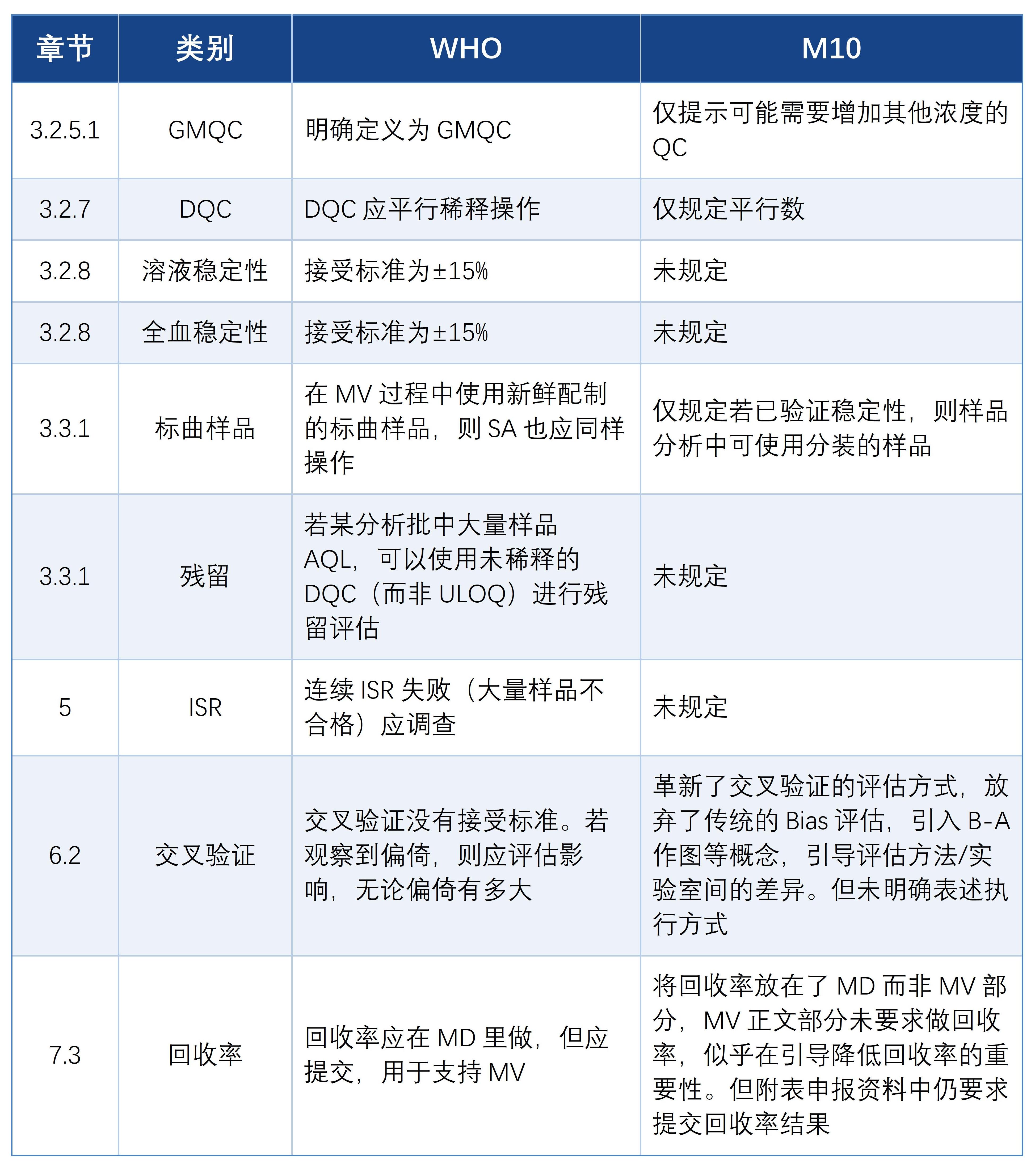
通過(guò)以上對(duì)比,可清晰看到兩份文件之間的差異點(diǎn),其中部分內(nèi)容可能需要特殊關(guān)注。
在生物分析法規(guī)不斷更新的當(dāng)下,有濟(jì)醫(yī)藥始終保持敏銳的洞察力,以積極的姿態(tài)緊跟法規(guī)動(dòng)態(tài)。我們嚴(yán)格遵循 ICH M10 以及各國(guó)最新的法規(guī)要求,憑借先進(jìn)的檢測(cè)技術(shù),為臨床生物樣品檢測(cè)提供精準(zhǔn)、可靠的服務(wù)。無(wú)論是在法規(guī)遵循還是技術(shù)能力上,有濟(jì)醫(yī)藥都展現(xiàn)出了專(zhuān)業(yè)的態(tài)度和卓越的能力,持續(xù)為臨床藥代動(dòng)力學(xué)研究提供高質(zhì)量的數(shù)據(jù)支持,助力新藥研發(fā)加速前行。