NDC藥物(包括抗體偶聯藥物ADC、多肽偶聯藥物PDC等)代表了靶向治療的重要發展方向。這類藥物的基本設計理念是:通過連接子將高細胞毒性的Payload與靶向配體(抗體或多肽)偶聯,實現精準遞送,最終殺傷腫瘤細胞。 目前,NDC藥物的研發呈現出多元化格局。ADC領域已經較為成熟,截至目前已有超過15款ADC藥物獲得FDA批準上市,涵蓋HER2、Trop-2、CD79b等多個靶點,廣泛應用于乳腺癌、淋巴瘤、尿路上皮癌等多種惡性腫瘤的治療。PDC作為新興方向,近年來也取得了重要進展,已有Pepaxto(melflufen)等藥物進入臨床并獲加速批準,雖然后續因臨床研究失敗而撤市,但PDC憑借其分子量小、腫瘤穿透力強、合成成本低等優勢,仍被視為下一代靶向治療的有力候選者。 與ADC不同,PDC的分子量更小(通常2-10 kDa),作用機制更加靈活多樣:可以通過受體介導的內吞進入細胞,在溶酶體或胞漿中釋放Payload;可以利用細胞穿透肽直接跨膜入胞,不依賴受體識別;可以在腫瘤微環境(低pH、高GSH、特異性酶)中釋放Payload,Payload再進入細胞發揮作用;或者作為整體復合物直接發揮藥效(如Lutathera);甚至可以靶向膜表面受體,在不進入細胞、不釋放Payload的情況下直接調節生物學功能(如Bicycle Therapeutics的雙環肽PDC—BT7480)。機制上的靈活性意味著其ADME特性更加復雜多變,對DMPK研究提出了更高要求。 然而,在NDC藥物的研發實踐中,一個令人困惑的現象反復出現:連接子設計精妙,藥效結果卻不及預期;考察體內過程時發現,藥物在血漿中穩定性良好,卻難以在靶點部位有效積累;深入追蹤代謝命運時更觀察到,母藥快速消失,游離Payload卻寥寥無幾。 這些困境的背后,折射出一個共性問題:我們只知道藥物進入了體內,卻不知道它去了哪里、變成了什么、為何沒能發揮作用。常規的母藥定量和總Payload測定,無法回答這些問題。而代謝產物鑒定(MetID),正是照亮這段黑暗旅程的那盞探照燈。 通過系統追蹤NDC分子在體內的代謝足跡,MetID能夠直接鑒定那些被常規檢測忽略的關鍵代謝物,為理解藥效、指導優化提供不可替代的證據。本文結合近年來的研究案例,梳理代謝產物鑒定在NDC藥物研究中的多重價值。
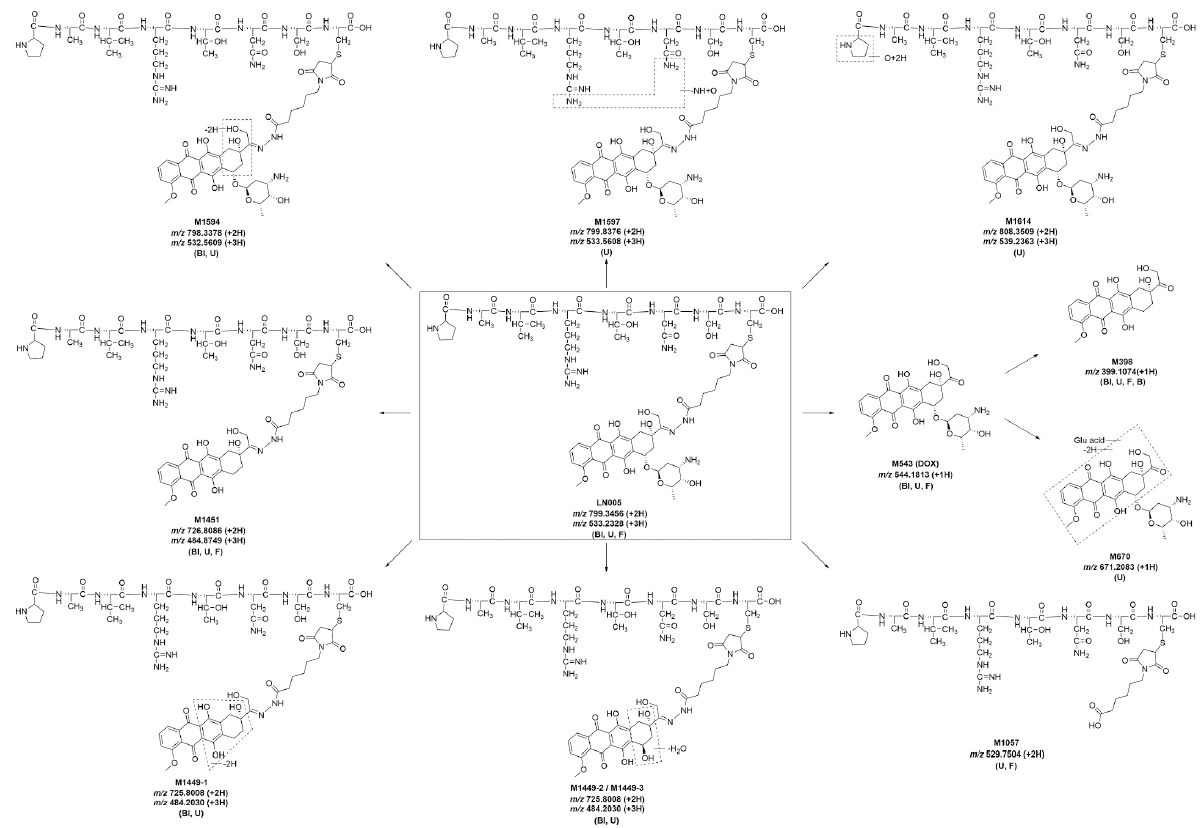
1 揭示Payload釋放后的真實形式:發現“活性喪失”的根源 連接子斷裂只是第一步,釋放后的Payload以什么形式存在,直接決定了其能否發揮藥效。有時,研究者雖然觀察到藥效不及預期,但常規檢測只能測量總Payload濃度,無法區分Payload是以游離活性形式存在,還是以其他形式被禁錮或失活。而MetID能夠直接鑒定釋放產物的化學結構,揭示那些隱藏在藥效數據背后的關鍵代謝物。 案例:c(RGDfC)-SS-DOX為何藥效不佳? Liang等構建的RGD靶向PDC體系中,研究者采用三種不同連接子將環狀RGD肽(c(RGDfC))與DOX偶聯[1]: c(RGDfC)-SS-DOX:可還原二硫鍵連接子 c(RGDfC)-S-DOX:不可切割的單硫鍵連接子 c(RGDfC)-VC-DOX:組織蛋白酶B可切割的纈氨酸-瓜氨酸二肽連接子 核心發現: 體外細胞毒性試驗結果顯示:c(RGDfC)-S-DOX和c(RGDfC)-VC-DOX的藥效是c(RGDfC)-SS-DOX和游離DOX的1.4-2.0倍[1] 通過共聚焦激光掃描顯微鏡(CLSM)等分析手段,研究者發現c(RGDfC)-SS-DOX在細胞內環境中會產生含巰基的DOX衍生物(DOX-SH),而其他連接子則釋放游離DOX[1] 這個案例說明了什么?二硫鍵連接子設計本意是在細胞內高GSH環境中快速釋放Payload,但實際釋放出的卻是DOX-SH這種異常形式的Payload。雖然“釋放”發生了,但“釋放的形式不對”,導致藥效不升反降。這一發現揭示了PDC研究中一個關鍵問題:Payload釋放后的化學形式,與釋放本身同等重要。 MetID的價值:該研究通過CLSM等手段觀察到了DOX-SH的存在,并基于此解釋了不同連接子藥效差異的原因。這一發現恰恰說明了在NDC研發中,識別Payload釋放后的真實化學形式至關重要。而在藥物研發實踐中,代謝產物鑒定(MetID)是發現和確證藥物相關產物最有力、最直接的手段。當我們在自己的NDC項目中遭遇“釋放率不低、藥效卻不高”的困境時,MetID就是追問“釋放出來的究竟是什么”的核心工具——它能夠系統性地發現那些可能被常規檢測忽略的異常代謝物,為理解藥效提供確鑿的分子層面證據。 2 描繪完整的代謝足跡:發現“中途下車者” NDC分子在體內的命運,遠比“連接子斷裂釋放Payload”這個簡單模型復雜得多。通過系統追蹤藥物在血漿、尿液、膽汁、糞便中的所有代謝產物,MetID能夠描繪完整的代謝足跡,發現那些從未到達靶點的“中途下車者”。 案例:LN005的11個代謝物 LN005是一款由靶向多肽VAP與阿霉素(DOX)通過pH敏感連接子偶聯而成的PDC候選物,靶向腫瘤內質網高表達的GRP78蛋白。 研究者采用UHPLC-HRMS技術,對大鼠靜脈注射LN005后的血漿、尿液、糞便和膽汁樣本進行了系統代謝物鑒定。這是首次對PDC藥物LN005在大鼠體內的代謝產物進行系統研究,共發現11個可能的代謝物[2]。 圖1. LN005大鼠靜脈注射18 mg/kg的代謝圖譜[2] 研究還發現,LN005的代謝與DOX密切相關,主要代謝途徑包括:氧化脫氨或水解、還原性糖苷鍵裂解、水解性糖苷鍵裂解和脫氫反應[2]。 MetID的價值:如果沒有MetID,研究者只會看到“血漿中母藥濃度下降”的數據,卻無法知道這些母藥究竟去了哪里——是被靶組織攝取并成功釋放Payload,還是在循環或肝臟中被提前代謝清除?LN005的研究通過系統代謝物鑒定,直接揭示了藥物在血液氧化代謝、肝臟攝取和膽汁排泄等多條“中途下車”路徑。 3 解析ADC的復雜代謝產物:發現“含Payload代謝物(PCCs)”的全貌 ADC藥物的代謝產物鑒定面臨獨特挑戰:含Payload代謝物(Payload-Containing Catabolites, PCCs)濃度低、結構未知、分子量范圍寬。MetID技術的進步正在突破這些瓶頸,為ADC的Payload設計和臨床前評價提供關鍵支持。 案例:T-DM1的含Payload代謝物研究 T-DM1(ado-trastuzumab emtansine)是一款經典的以DM1為Payload、以不可裂解連接子(MCC)構建的ADC。蔡婷婷等研究者開發了一種基于LC-HRMS的通用方法,用于系統鑒定不可裂解ADC的體外PCCs[4]。 研究設計: 將T-DM1和另一款ADC-1分別與人肝臟溶酶體、肝臟S9組分及腫瘤細胞共孵育 采用高分辨質譜結合兩種數據挖掘工具:非靶向背景扣除(PATBS)和靶向產物離子過濾(PIF) 系統鑒定所有含Payload的代謝產物 核心發現: 在T-DM1的人肝臟溶酶體孵育體系中,共檢測并結構表征了多種PCCs 這些PCCs的大多數由MCC-DM1與幾個氨基酸組成——即連接子-MCC與Payload DM1形成的綴合物上,連接著不同數量的氨基酸殘基 ADC-1在多個物種(人、大鼠、猴)肝臟S9及腫瘤細胞中,生成1個主要PCC和3個次要PCC,驗證了Payload設計的合理性 MetID的價值:該研究系統揭示了不可裂解ADC在溶酶體中的代謝命運——抗體部分被逐步降解,留下“連接子-Payload-氨基酸殘基”形式的PCCs。這些PCCs本身可能具有藥理活性,其生成和積累直接影響ADC的藥效和毒性。如果沒有MetID,研究者將無法發現這些PCCs的存在,也無法理解不可裂解ADC的活化機制。這一案例充分展示了MetID在支持ADC早期研發、指導Payload設計中的關鍵作用。 4 建立種屬橋接,預判臨床風險 NDC藥物的臨床前研究依賴于動物模型,但不同物種之間的代謝差異可能導致臨床轉化失敗。MetID可以在臨床前階段建立“代謝的種屬相關性”,為首次人體試驗的風險評估提供關鍵依據。 案例1:ADC-1的種屬比較 在上述ADC研究中,研究者同時考察了ADC-1在不同物種肝臟S9中的代謝譜[4]。 核心發現: ADC-1在人、大鼠、猴的肝臟S9孵育中均生成相同的1個主要PCC和3個次要PCC 代謝譜在三個物種之間高度一致 MetID的價值: 動物模型的可靠性:如果在動物模型中觀察到ADC的代謝行為,且代謝譜與人相似,那么動物模型的結果對于預測人體代謝具有重要參考價值 Payload設計的驗證:跨物種代謝譜的一致性,驗證了該Payload設計在不同物種中具有相似的代謝命運 臨床風險的早期預警:在臨床前階段就能了解ADC分子在不同物種中的代謝特征,為后續研究設計提供依據 案例2:LN005的種屬比較 PDC同樣適用這一思路。LN005的體外研究采用不同物種的肝臟S9組分孵育,發現了4個主要代謝物,主要代謝途徑為氧化脫氨或水解。更重要的是,代謝譜在小鼠、大鼠、犬、猴和人之間高度相似[3]。 MetID的價值: 代謝途徑的可預測性:氧化脫氨和水解是跨物種保守的代謝通路,應作為NDC設計的重點關注對象 臨床轉化的信心:跨物種代謝譜一致,為后續臨床研究提供了重要依據 5 指導結構優化的“靶點地圖” MetID不僅能夠解釋代謝途徑,更能指導結構優化。通過明確主要代謝途徑和代謝脆弱位點,MetID為化學家提供了優化的精準方向。 來自PDC的啟示:LN005的主要代謝途徑 LN005的研究明確指出了主要代謝途徑——“氧化脫氨或水解”[2,3]。這些位點正是結構優化的靶點: 在易氧化位點引入空間位阻 用非天然氨基酸替代敏感殘基 來自ADC的啟示:T-DM1的PCCs結構特征 T-DM1的PCCs結構表征揭示了一個關鍵特征:PCCs由MCC-DM1與不同數量的氨基酸殘基組成[4]。這提示: 不可裂解ADC的活性形式可能不是游離Payload,而是“連接子-Payload-氨基酸”綴合物 在設計不可裂解ADC時,需要關注這種綴合物的活性和透膜能力 避免產生含巰基的Payload(如DOX-SH案例所示) 沒有MetID提供的代謝途徑信息,結構優化只能是盲目的“試錯”。 6 結語:讓每一個NDC的“體內足跡”都清晰可見 從c(RGDfC)-SS-DOX研究中通過CLSM等手段發現的含巰基DOX衍生物[1],到LN005研究中通過UHPLC-HRMS直接鑒定的11個代謝物[2,3],再到T-DM1研究中系統發現的多種含Payload代謝物[4],這些案例共同指向一個核心結論: NDC在體內的命運,遠比“連接子斷裂釋放Payload”這個簡單模型復雜得多。常規檢測只問“母藥還剩多少”“總Payload有多少”,但MetID能追問“釋放出的Payload是什么形式”“藥物整體去了哪里”“變成了什么”。 當研究者發現二硫鍵連接子釋放出的不是游離DOX而是DOX-SH時[1],當研究團隊在LN005的糞便中發現超過一半的LN005相關物質以水解產物形式存在時[2],當研究者系統鑒定出T-DM1的多種PCCs并揭示其由MCC-DM1與氨基酸殘基組成時[4],這些發現都指向同一個事實:NDC在體內可能生成多種Payload之外的分子,而這些“隱藏”的代謝物是理解藥物體內過程的關鍵。 這正是代謝產物鑒定在NDC研發中的核心價值:作為發現和確證藥物相關產物最有力的手段,它讓研究者能夠系統性地揭示那些被常規檢測忽略的代謝物,為理解藥物的體內命運提供分子層面的證據。 科學的DMPK策略,是“因時制宜”的精準設計 在NDC藥物研發的長周期中,DMPK研究不應是僵化的“標準操作”,而應是基于科學認知的“動態適配”。在早期篩選階段,應聚焦Payload本身的屬性,合理看待母藥數據的局限性——這是基于機制認知的理性選擇;在PCC確認階段,則需要攻堅克難、建立可靠的MetID方法,這是對藥物研發負責的必經之路。而貫穿始終的MetID策略,正是連接這些階段的橋梁——它讓研究者能夠全面追蹤藥物的代謝足跡,發現那些影響藥效的“隱藏變量”,為理解每一個分子的體內過程提供關鍵證據。 有濟醫藥DMPK部門深耕偶聯藥物領域多年,在PDC、ADC等NDC新型藥物的體外ADME研究、體內PK研究及復雜樣品分析方面積累了豐富的實戰經驗。我們不僅提供標準化的DMPK服務,更致力于與申辦方一同探討基于項目階段、分子特性的科學定制化研究策略,將MetID等先進工具融入研發全流程。讓我們攜手,以更智慧的DMPK策略,助力NDC藥物研發之路行穩致遠。 參考文獻 [1] Liang Y, Li S, Wang X, et al. A comparative study of the antitumor efficacy of peptide-doxorubicin conjugates with different linkers. Journal of Controlled Release. 2018;275:129-141. [2] Wang W, Chen C, Luo J, et al. Metabolism investigation of the peptide-drug conjugate LN005 in rats using UHPLC-HRMS. Journal of Pharmaceutical and Biomedical Analysis. 2024;238:115860. [3] Yuan Y, Wang W, Luo J, et al. Metabolite characterisation of the peptide-drug conjugate LN005 in liver S9s by UHPLC-Orbitrap-HRMS. Xenobiotica. 2024;54(1):1-9. [4] Cai T, Shi L, Guo H, et al. Detection and Characterization of In Vitro Payload-Containing Catabolites of Noncleavable Antibody-Drug Conjugates by High-Resolution Mass Spectrometry and Multiple Data Mining Tools. Drug Metabolism and Disposition. 2023;51(5):591-598.