在全球藥物研發格局中,大分子生物藥與小分子藥物形成鮮明技術路徑差異。小分子藥物多通過化學合成制備,作用靶點寬泛、脫靶效應相對較高,且易受細胞屏障限制;而大分子生物藥(如治療性蛋白/多肽、單克隆抗體、病毒載體基因治療藥物、ADC藥物等)依托生物合成技術,以靶向性強、療效確切、治療窗口寬為核心優勢,能精準穿透疾病關鍵通路,為腫瘤、自身免疫性疾病、罕見病等難治性疾病提供突破性治療方案,已成為創新藥研發的核心賽道。
但由于大分子生物藥多具有異源性或復雜大分子結構,易誘導機體產生免疫原性,進而形成中和抗體(NAb)。中和抗體可通過阻斷藥物到達靶標或干擾受體/配體結合,直接削弱藥物體內活性,不僅可能導致治療失效,還可能引發交叉免疫反應等安全風險,因此中和抗體檢測已成為大分子生物藥研發與臨床應用必不可少的一部分。
一、中和抗體的考察場景
臨床研究階段:需滿足NMPA、FDA等監管機構申報要求,支撐給藥方案優化與療效相關性分析; 臨床應用階段:患者出現療效不佳、治療失效或免疫相關不良反應時,需通過檢測排查中和抗體影響; 特殊藥物需求:基因治療藥物給藥前需篩查患者預存中和抗體,避免載體被清除; 一致性評價:生物類似藥上市前后需對比原研藥免疫原性特征,證明臨床安全性與有效性一致性。
二、CBA方法開發考量點
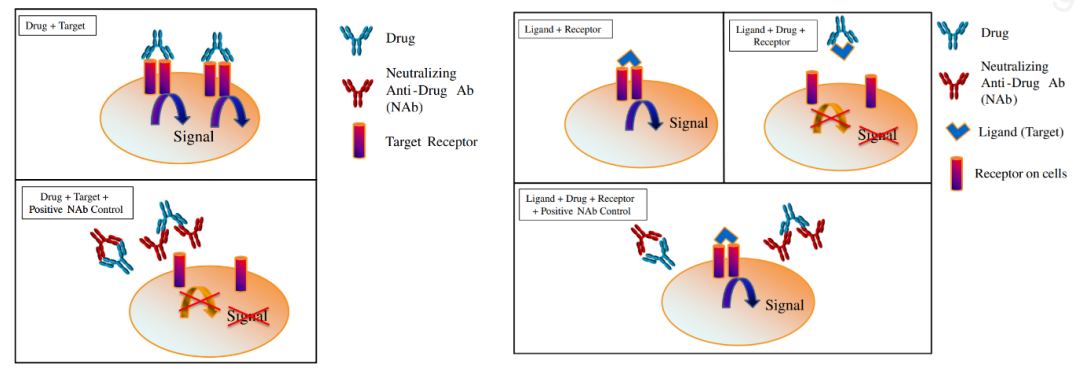
直接法采用表達靶受體的細胞系,通過檢測藥物分子與其同源受體直接相互作用所誘導的檢測信號來實現,中和抗體可阻斷藥物功能,使檢測信號減弱,反應原理如圖1(左)[1]。間接法除藥物和適配細胞系外,通常還需配體等額外組分(配體可與細胞同源受體結合),配體與受體相互作用可產生檢測信號,藥物會中和配體并使檢測信號降低,而中和抗體可抑制藥物的這一中和功能,使檢測信號恢復,反應原理如圖1(右)[1]。
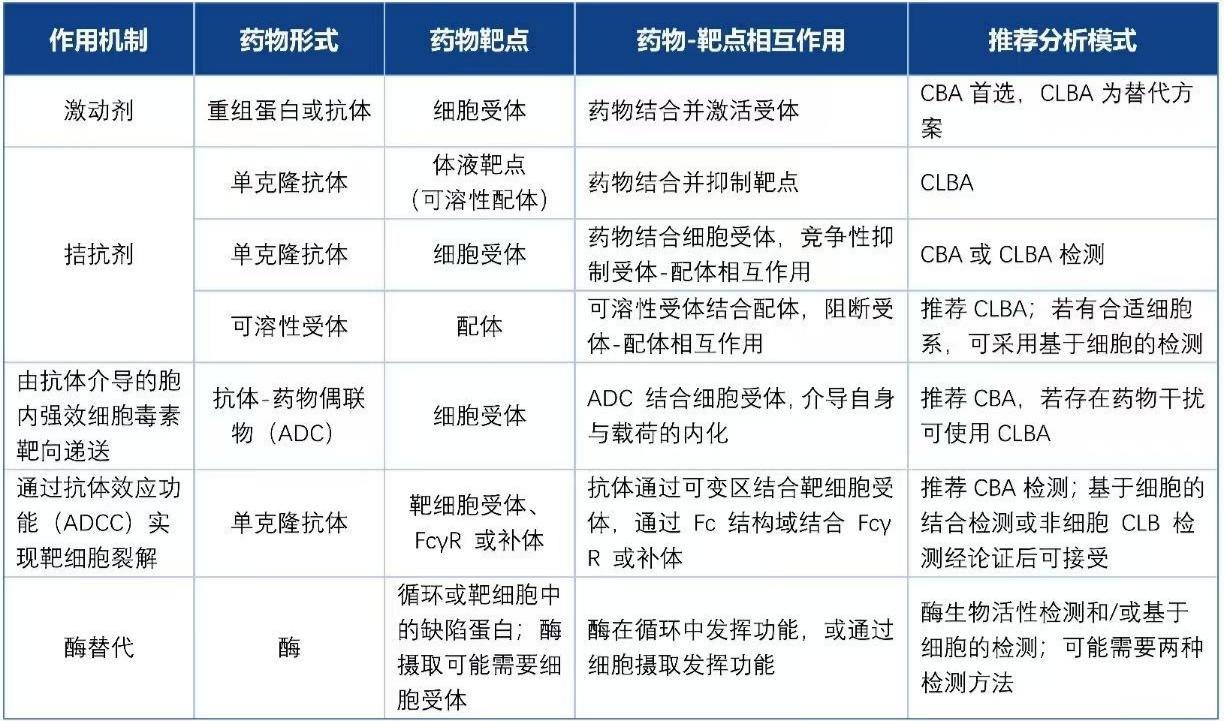
一般來說CBA法被監管部門認為是衡量藥物產生中和抗體的金標準,但在法規上未做強制要求。根據藥物的類型和作用機理、免疫原性風險、方法本身的選擇性、基質干擾程度、靈敏度等選擇分析模式,匯總結果見表1[1]。
采樣時間避開藥物體內濃度峰值,最好采集藥物谷濃度樣本。 血清預處理,通過物理方式去除或降低血清中的藥物濃度。 調整試驗參數,如調整樣本MRD、孵育時間、細胞密度、藥物干擾檢測信號時更換檢測方法等。為了保證試驗的可重復性及準確性,整個實驗過程最好使用同一品牌、同一貨號的試劑,比如培養基、胎牛血清、檢測試劑盒等,如有可能盡量避免使用不同批次的試劑,減少批次帶來的信號波動。試驗耗材也需確保無菌,避免影響細胞活性或抗原抗體結合。
三、Nab方法驗證內容
方法開發完成后,需對方法進行完整驗證,主要包括臨界值、鉤狀效應、精密度、選擇性、靈敏度、耐藥性、穩健性等[2-6]。方法臨界值一般采用固定臨界值,當試驗存在明顯變異時,也可采用浮動臨界值。靈敏度無具體規定,可參考ADA的指導原則。不同于ADA的穩健性驗證,NAb還需額外考慮細胞傳代數、培養基批次對結果的影響。
中和試驗一般僅對ADA檢測為陽性的樣本進行檢測,通常不進行確證試驗。對于ADA陽性樣本檢測一般采用1%的假陽性率,當使用中和活性對個體進行篩選時,應采用5%假陽性率[2]。
四、案例分析:GLP-1/GIP受體激動劑NAb檢測
目前全球已有1個GLP-1/GIP雙重受體激動劑獲批上市,多個GLP-1/GIP、GLP-1/GCG雙重和GLP-1/GIP/GCG三重受體激動劑處于臨床開發階段。
有濟醫藥針對GLP-1及GIP分別建立了基于CBA法的NAb檢測方法,選擇了高表達人GIPR受體的細胞株以及高表達人GLP1R受體的細胞株,通過GIPR激動劑或GLP1R刺激劑驅動熒光素酶表達系統。在沒有激動劑的情況下,GIPR/GLP1R受體不被激活,發光信號低。在激動劑存在的情況下,以劑量依賴的方式檢測到GIPR/GLP1R途徑激活的發光。
細胞種板培養,待測樣本經過預處理后與一定濃度的藥物共孵育,一同加入細胞中,藥物與細胞表面的靶點結合,刺激細胞產生熒光素酶。有NAb存在時,NAb與藥物結合阻斷藥物與細胞表面的靶點結合,最后加入熒光素酶檢測試劑,信號強度與樣品中NAb的濃度在一定范圍內呈負相關。
通過對細胞鋪板密度(見圖2)、孵育時間的優化,在不同藥物濃度下確定了EC50,GIP藥物響應曲線如圖3所示,GLP-1藥物響應曲線如圖4所示。方法開發過程中,發現LPC濃度下藥物耐受大約為100 ng/mL,PK檢測結果顯示最高藥物濃度大約為450 ng/mL,藥物耐受水平差會導致假陰性結果,通過優化成功將耐藥性提高至850 ng/mL,提高了檢測的準確性。對方法進行完整驗證,包括臨界值、靈敏度、鉤狀效應、精密度、藥物耐受性、選擇性、系統適用性、穩健性的考察,各項指標均符合接受標準。
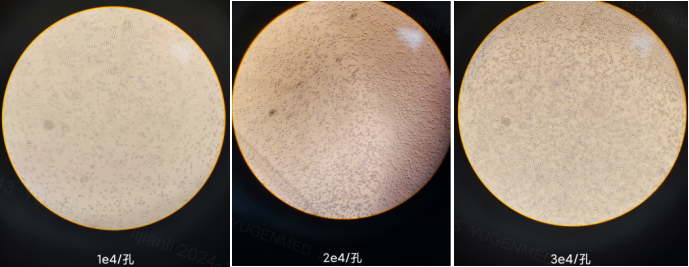
圖2 細胞密度的選擇
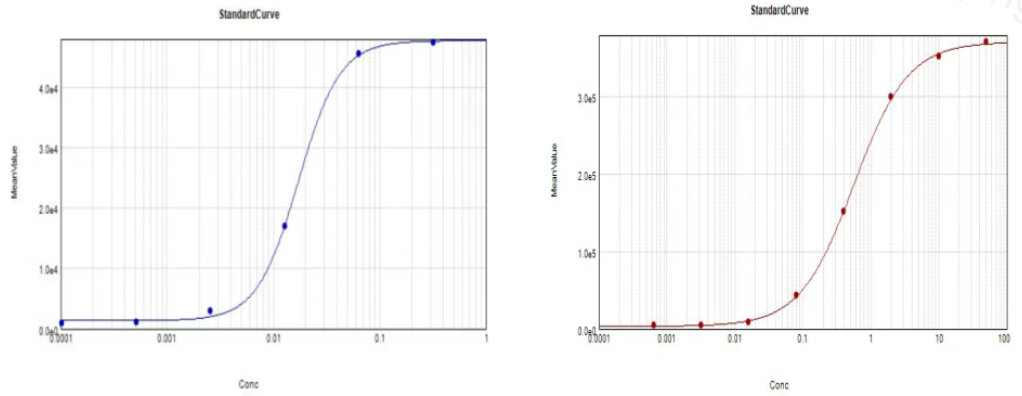 圖3 GIP藥物響應曲線;圖4 GLP-1藥物響應曲線
圖3 GIP藥物響應曲線;圖4 GLP-1藥物響應曲線結語
有濟醫藥已建成覆蓋多類大分子生物藥的中和抗體檢測平臺,具備從細胞系篩選、方法開發、全項驗證到樣品檢測的一站式服務能力,以高特異性、高靈敏度、高合規性的技術方案,助力創新生物藥加速上市進程。