隨著小分子藥物、生物制品以及新型治療手段的快速發展,藥物在體內的代謝過程日趨復雜。在藥物研發的非臨床階段,系統鑒定體內外代謝產物是預測人體暴露風險、指導毒理種屬選擇及優化臨床試驗設計的關鍵環節。
根據ICH M3(R2)指導原則,若人體循環中某一代謝物的暴露量超過母體藥物總相關物質AUC的10%(即MIST閾值),且其在人體中的暴露量水平顯著高于毒理學試驗動物中的最大暴露量,則表明所用動物種屬未能充分覆蓋該人體代謝物,此時需針對該代謝物另行開展非臨床安全性評價。美國FDA 2020年發布的《Safety Testing of Drug Metabolites》指導原則進一步強調,應通過體外跨種屬比較驗證毒理種屬對關鍵代謝物的覆蓋能力。我國NMPA在《藥物代謝產物安全性試驗技術指導原則》中要求盡早進行代謝差異比較與分析,以決定是否開展安全性評價。為了更全面地理解藥物的代謝行為,通常需綜合運用多種實驗體系,對體內外代謝產物進行定性與半定量分析。下文將系統介紹常用體外與體內代謝實驗體系的特點及應用策略。
體外代謝實驗體系是模擬藥物體內生物轉化過程的重要工具,可用于識別主要代謝產物及其代謝途徑。體系選擇需綜合考慮研究目的、藥物特性(如分子類型、理化性質)及目標代謝通路的覆蓋范圍。下文總結了常用體外代謝體系(按復雜性遞增:從簡單、機制明確到復雜、生理相關)及其特點與應用策略。目的:明確特定代謝酶(如單個CYP450亞型、UGT、SULT等)對化合物的代謝作用。特點:表達單一特定的代謝酶(如CYP3A4、UGT1A1),體系純凈,背景干擾低,易于生成單一、純凈的代謝物。局限性:酶活性水平遠高于生理濃度,缺乏體內復雜的酶協同或競爭作用,結果外推至體內需謹慎。
- 鑒定特定酶(如某個CYP或UGT亞型)介導的代謝途徑;
- 作為其他體系(如微粒體、肝細胞)代謝途徑研究的靶向驗證工具。
目的:評估化合物在對應器官微粒體中的I相代謝穩定性、代謝產物譜及主要參與代謝的CYP亞型等。特點:富含I相代謝酶(如細胞色素P450酶系)和部分II相代謝酶(如尿苷二磷酸葡萄糖醛酸轉移酶,UGT),應用廣泛、標準化程度高、酶含量高、操作簡便和成本較低,適用于高通量篩選。局限性:缺乏完整細胞結構,II相代謝酶含量較低(除UGT外),無法模擬藥物的完整攝取、轉運及分泌過程,可能低估結合型代謝物(如硫酸酯、谷胱甘肽結合物)的生成。
- 通常在單體酶確認關鍵酶后,用于研究其在更接近生理的酶混合物環境中的代謝行為;
- 作為I相代謝(尤其是CYP450介導)研究的黃金標準和核心工具;
- 除肝微粒體外,亦可使用肺、腸、腎等器官來源的微粒體開展器官特異性代謝研究。
目的:評估包含I相(CYP450等)和II相(UGT、SULT、GST等)代謝酶在內的更全面代謝穩定性與代謝產物譜。特點:包含完整的I相和II相代謝酶(包括胞漿酶),可同時發生氧化、還原、水解和結合反應,并可模擬溶酶體酸性環境,代謝潛力覆蓋更全面。局限性:酶濃度和活性通常低于微粒體或胞漿,背景雜質較多,代謝速率較慢,難以大量生成代謝物。
- 當懷疑有重要胞漿酶(如AO、XO、SULT、GST等)參與代謝或需同時考察I相和II相代謝時選用;
- 作為多肽-藥物偶聯物(PDC)和核酸類藥物代謝研究的初篩補充體系,用于評估水解酶介導的降解或酸性環境穩定性,但需結合更生理相關的體系(如原代細胞、胞漿)進行關鍵機制驗證。
目的:評估化合物是否被特定胞漿酶代謝(如硫酸化、谷胱甘肽結合),研究相應酶動力學。特點:主要含有可溶性II相代謝酶(如谷胱甘肽-S-轉移酶,GST;N-乙酰基轉移酶,NAT;硫酸基轉移酶,SULT;醛酮還原酶,AKR),無膜結構干擾,酶活性位點直接暴露。局限性:完全缺乏I相代謝酶,僅覆蓋特定II相代謝途徑(如谷胱甘肽結合、硫酸化、乙酰化),代謝途徑單一,應用場景受限。
- 專門研究特定II相代謝途徑(如SULT、GST等)或需可溶性輔因子的酶(如ALDH);
- 生成特定II相代謝物標準品;補充微粒體或S9體系的研究結果。
目的:模擬藥物在完整、有活力細胞內的整體代謝處置過程。特點:原代細胞(如原代肝細胞)保留完整的細胞結構,含豐富的I相和II相酶(如CYP、UGT、AO、FMO、SULT、GST等),具有最高的生理相關性。局限性:制備復雜,成本高昂,細胞活性隨時間下降較快。
- 引入了細胞完整性、轉運體、內源性輔因子、酶的空間分布等更接近體內環境的因素,是評估藥物整體代謝命運(攝取、代謝、外排)的金標準體系;
- 通常在亞細胞組分(微粒體/S9)篩選后,用于評估更綜合的代謝行為。
目的:通常用于研究化合物在組織(如腸、腎、肺、腦、皮膚)的代謝穩定性與代謝產物譜,識別潛在的組織特異性毒性或活化。特點:保留了所有細胞器及酶系(包括I相和II相酶),最接近體內的生理環境。局限性:背景干擾較大(含細胞碎片、內源性物質多),對分析技術要求較高,酶活性可能不如純化體系穩定。
- 當關注化合物在特定靶器官或首過代謝器官(如腸道)的局部代謝時使用;
- 核酸類藥物(如短干擾核糖核酸、小干擾RNA (siRNA)、反義寡核苷酸 (ASO)等)代謝研究常用體系(如肝、腎勻漿)。
腫瘤組織勻漿(Tumor Homogenates)目的:評估抗腫瘤藥物在目標腫瘤組織中的代謝穩定性(是否被腫瘤細胞快速滅活)或研究前藥在腫瘤組織中的活化特性(如通過腫瘤特異性酶的作用)。此外,研究腫瘤微環境(如酸性環境)對藥物代謝行為的影響。特點:直接針對靶組織,可能揭示腫瘤特異的代謝途徑(如某些腫瘤高表達的酶)。局限性:樣本獲取困難(通常來自手術或活檢)、個體差異大(腫瘤異質性)、制備和標準化困難(勻漿程度、酶活性保持)。
- 識別和鑒定僅在腫瘤組織勻漿中出現或在腫瘤組織中顯著增強的代謝產物,從而發現潛在的腫瘤特異性代謝酶或通路;
血漿/全血(Plasma/Whole Blood)目的:評估化合物在血漿/全血中是否被酶解(如酯酶、肽酶)。特點:專門用于評估血漿/全血中水解酶(如酯酶CES、肽酶)介導的代謝行為。它能夠反映化合物在血漿/全血中的特異性失活途徑,操作簡單,并且無需添加輔酶因子。局限性:僅適用于評估水解代謝途徑,種屬差異顯著。例如,酯酶活性在動物與人類之間存在極大差異,因此臨床預測必須使用人源血漿/全血,而動物血漿僅適用于輔助機制研究。
- 驗證前藥的活化或穩定性優化,探索藥物在血漿中的活化與失活機理;
- 化合物在血液/血漿中的穩定性研究及代謝產物快速篩選;
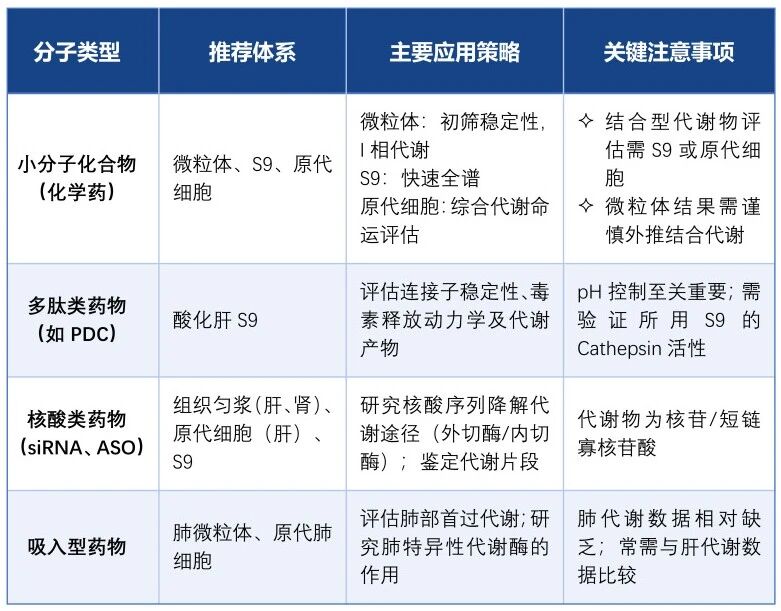
下表總結了不同分子類型推薦的體外代謝實驗體系、應用策略及關鍵注意事項:
在早期研發階段,多采用上述體外體系進行跨物種代謝物譜對照,確認所選物種可覆蓋人體代謝物。若發現動物中無或低量存在人特異性代謝物,則需重點關注該代謝物的毒性風險。
在毒理學或藥代動力學研究過程中,收集血漿、尿液、糞便等樣本,通過LC-UV-HRMS等方法分析藥物及其代謝物譜。常用嚙齒類(小鼠、大鼠)和非嚙齒類(犬、靈長類)動物進行研究,通過不同物種的體內代謝譜對比,可以初步判斷所選物種是否覆蓋人體代謝特征。
根據藥物研發的不同階段,應合理組合使用上述實驗體系:
主要使用肝微粒體和懸浮肝細胞等體外體系快速評估候選化合物的代謝途徑。在此階段,常跨物種使用人、鼠、犬、猴的肝微粒體或肝細胞,篩選體外代謝產物并比較譜圖,初步識別代謝軟點,指導化合物結構優化。若早期發現化合物代謝率慢或存在特殊代謝途徑,可使用更完善的體外體系進行深度分析。例如,對于慢速代謝物,可采用貼壁培養的肝細胞或懸浮肝細胞接力孵育法以延長孵育時間;對于產生反應性代謝物的化合物,可在微粒體/S9體系中加入GSH/Cys等捕獲劑,評估化合物的潛在毒性風險。此外,可借助重組CYP/UGT酶體系鑒定具體酶亞型的代謝產物和貢獻度。在毒理學的動物種屬選擇時,進行跨物種體外代謝物譜對比和有限的動物體內代謝研究,確保所選擇的物種可覆蓋人體代謝情況。代謝實驗體系的選擇應以化合物結構、物理化學性質和已知代謝途徑為依據。對于疏水性較大、膜透過性較好的化合物,可優先使用懸浮肝細胞測試;若預測主要通過CYP酶代謝,則首選肝微粒體;針對已知主要代謝酶,可使用重組酶進一步驗證其代謝產物結構。合理的實驗設計通常采取“由單一體系到多體系、先體外后體內”的遞進式策略,以覆蓋盡可能多的代謝產物。不同物種之間的代謝酶譜存在顯著差異,導致代謝物譜在定性和定量上可能存在較大差異。例如,某些CYP亞型在人類、犬和鼠中的表達量不同,使得人特異代謝物僅在部分動物中出現(華法林在人體中由CYP2C9介導生成毒性代謝產物7-羥基華法林,在大鼠代謝研究中可檢測出該毒性代謝產物,而犬幾乎不產生7-羥基華法林)。因此,在選擇相關動物種屬時需充分考慮物種差異,通常建議在體外研究階段,采用人源及多種動物來源的肝細胞(或肝微粒體)進行平行評價,以提高體外至體內外推的可靠性及毒理評估的物種相關性。根據FDA-MIST指導原則,當人體血漿中發現高比例代謝物(>10%母體AUC)時,需與毒理動物的代謝物暴露進行對比。如果動物中缺少或暴露顯著低于人體的代謝物,則應在該動物或其他替代物種中進行額外的代謝物安全性研究。國家藥監局(NMPA)也鼓勵盡早開展人體放射性物質平衡研究,以全面了解藥物的代謝和排泄特征。2024年發布的技術指導原則明確指出,通過人體物質平衡研究可鑒定藥物在體循環中的代謝產物并測定其占比,為后續研發工作提供依據。因此,在開展非臨床研究時應緊密結合全球法規要求,在合適的時間節點使用相應體系獲得代謝物數據,以確保安全性評估的充分性。
非臨床階段藥物代謝產物研究需要綜合利用多種實驗體系,系統刻畫候選藥物的代謝命運。從體外肝微粒體、肝細胞、S9和重組酶體系到常規動物體內代謝研究,各體系各有側重,應根據藥物特性和開發階段合理組合使用。通過體外預測結合體內驗證,實現代謝物的全譜分析和安全性評估,從而滿足藥物開發和監管申報的需求。
在實際研究中,建議制定前瞻性的代謝研究策略,靈活調整實驗方案,確保關鍵代謝物在安全性研究物種和人體中得到充分覆蓋。有濟醫藥DMPK部門已建立完善的代謝產物研究平臺,使用LC-UV-HRMS(Q-Exactive或Q-TOF)高分辨液質聯用儀,在體內/外生物樣品中捕獲未知代謝物信號響應,結合專業數據分析解析軟件,快速完成結構推測。同時,我們還搭建了放射性同位素技術平臺,可承接3H、14C 、125I、99mTc 等放射核素標記物的非臨床與臨床相關研究,開展質量平衡、物質排泄途徑及代謝產物譜的定量與定性研究,全面揭示藥物在生物體內的代謝命運。兩大技術平臺相互支撐,共同為藥物研發提供全面、可靠的代謝信息支持。